Aktuelle Verordnungsinformation
Einführung eines Arzneimittelinformationssystem in die Praxissoftware ab Oktober 2020
02.10.20, 11:08
- Arzneimittel
Ab 1. Oktober 2020 wird ein Arzneimittelinformationssystem (AIS) gesetzlich* verpflichtender Bestandteil der Verordnungssoftware. Ziel ist es, die Informationen der Frühen Nutzenbewertung des Gemeinsamen Bundesausschuss (G-BA) dem Arzt während des Verordnungsvorgangs bereitzustellen.
Die Frühe Nutzenbewertung wird durch das IQWIG durchgeführt und vergleicht seit 2011 auf Basis der Zulassungsstudien neu zugelassene Präparate mit dem gültigen Therapiestandard, der sogenannten „zweckmäßigen Vergleichstherapie“. Auf Basis der wissenschaftlichen Bewertung durch das IQWIG wird der Zusatznutzen durch den G-BA beschlossen.
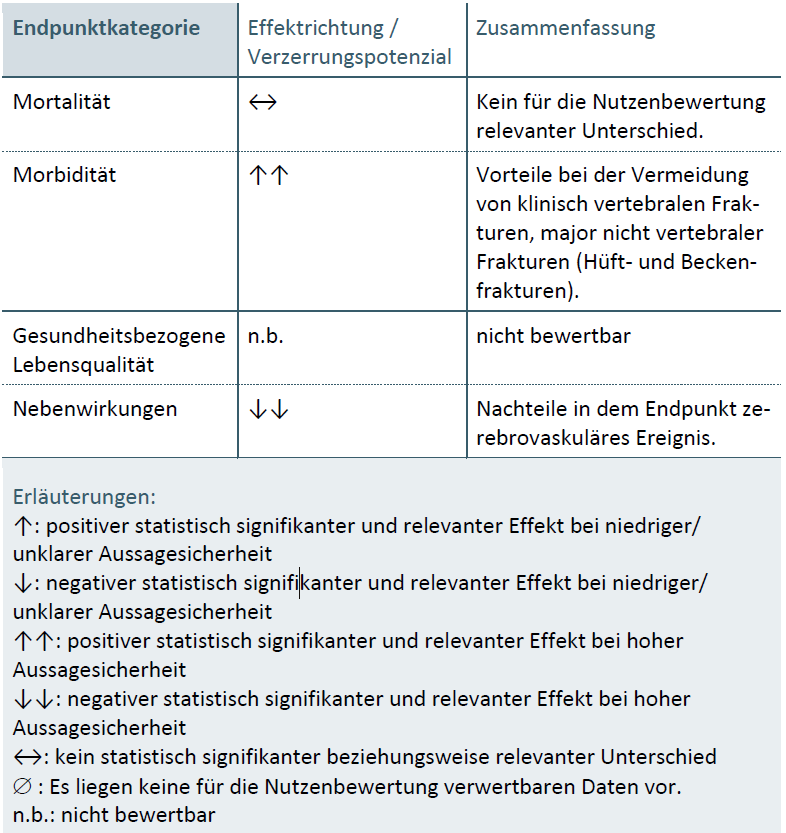
Klinisch relevante Endpunkte (z.B. Mortalität, Morbidität) werden grafisch dargestellt (Schnellüberblick). Der zugrunde liegende Beschluss des G-BA wird zusätzlich in der Software verlinkt. Zunächst werden die Beschlüsse des G-BA ab 1. Juli 2020 in der Verordnungssoftware abrufbar sein, ältere Beschlüsse sollen schrittweise bereitgestellt werden.
Eine Besonderheit bilden Präparate mit bedingter Zulassung und Mittel zur Behandlung seltener Erkrankungen (Orphan Drugs) dar. Der G-BA kann bei fehlender Evidenz zum Zeitpunkt der Frühen Nutzenbewertung eine Anwendungsbegleitende Datenerhebung fordern und festlegen, dass nur Teilnehmer dieser Studie das betroffene Arzneimittel verordnen können**. In diesem Fall wird ein entsprechender Hinweis in der Praxissoftware angezeigt.
* Elektronische Arzneimittelinformations-Verordnung (EAMIV) vom August 2019
** Gesetz für mehr Sicherheit in der Arzneimittelversorgung (GSAV)
Letzte Beiträge
Alle Informationen anzeigen
Lassen Sie sich mit einem Klick alle Verordnungsinformationen anzeigen: